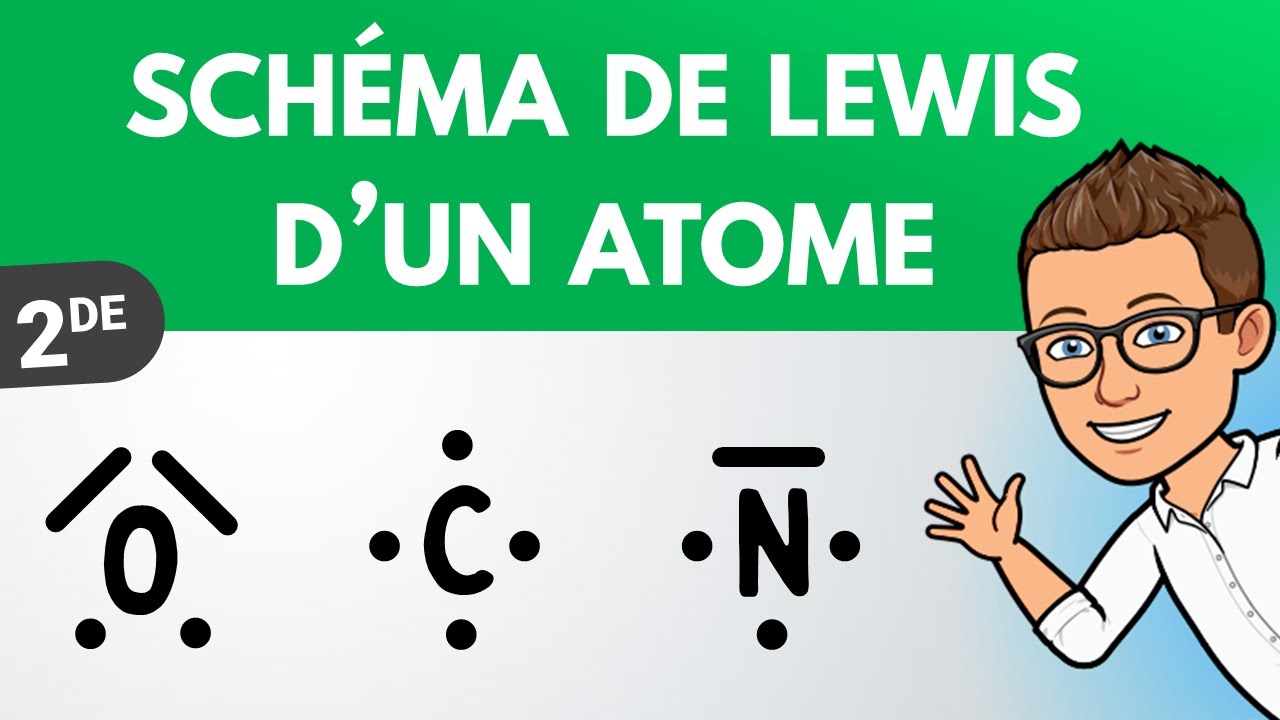
Comprendre la méthode de Lewis pour représenter une molécule
La méthode de Lewis est un outil essentiel pour visualiser les liaisons chimiques dans les molécules. Elle permet de représenter les électrons de valence de chaque atome et de montrer comment ils participent à la formation de liaisons chimiques. Cette méthode est particulièrement utile pour les élèves cherchant à comprendre les interactions atomiques de manière simple et directe.
Imaginez un atome comme une personne cherchant à se faire des amis pour atteindre le nombre idéal de huit amis, en accord avec la règle de l’octet 📜. C’est cette quête qui conduit à la formation de liaisons entre les atomes, créant ainsi une structure stable appelée structure de Lewis.
Les électrons de valence : les acteurs principaux
Les électrons de valence 🌀 sont ceux qui se trouvent sur la couche externe d’un atome. Ce sont eux qui participent aux liaisons chimiques. En utilisant des points autour des symboles chimiques, la méthode de Lewis illustre quelles paires d’électrons peuvent être partagées entre les atomes.
Par exemple, considérons une molécule simple comme H₂O. L’oxygène a six électrons de valence et a besoin de deux électrons supplémentaires pour compléter sa couche externe. Chacun des atomes d’hydrogène, avec un seul électron, comblera cet espace pour établir deux liaisons covalentes avec l’oxygène.
Sur le meme sujet
Donna Haraway, philosophe des sciences : « L’urgence de démilitariser le savoir à notre époque »
Donna Haraway et la Philosophie des Sciences Donna Haraway, une figure emblématique de la philosophie des sciences, a toujours su…
Étapes pour dessiner une structure de Lewis
Avant de se lancer dans la représentation d’une structure de Lewis, il est important de suivre certaines étapes méthodiques :
- 🔍 Identifier le nombre total d’électrons de valence disponibles.
- 📏 Disposer les atomes en déterminant l’atome central (généralement le moins électronégatif).
- 🔗 Dessiner les liaisons simples entre l’atome central et les autres atomes.
- ⚖ Répartir les électrons restants pour satisfaire la règle de l’octet.
Un exemple illustratif est le dioxyde de carbone (CO₂). Le carbone, étant l’atome central, établira une double liaison avec chaque atome d’oxygène pour compléter les octets de tous les atomes impliqués.
La règle de l’octet : un principe clé
La règle de l’octet stipule qu’un atome est le plus stable lorsqu’il est entouré de huit électrons dans sa couche de valence, à l’exception notable des atomes tels que l’hydrogène, qui est satisfait avec deux 📘. Ce principe guide la formation des liaisons dans de nombreuses molécules communes.
Exceptions notables à cette règle incluent les molécules comportant des atomes comme le phosphore ou le soufre, qui peuvent accueillir plus de huit électrons. Ces cas représentent des situations où une compréhension approfondie de la chimie d’extension est nécessaire.
Sur le meme sujet
Quelle science est considérée comme la plus facile et pourquoi
Comprendre la Perception de la Facilité en Sciences La question de savoir quelle science est perçue comme la plus facile…
Les liaisons chimiques et leurs représentations dans les structures de Lewis
Les différentes types de liaisons chimiques sont essentielles pour comprendre comment les atomes se regroupent pour former des molécules. Les exemples typiques incluent les liaisons covalentes simples, doubles et triples, symbolisées par des lignes simples, doubles ou triples entre les atomes respectifs.
Par exemple, la molécule de dioxygène (O₂) est représentée par une double liaison covalente entre deux atomes d’oxygène, tandis que l’azote (N₂) utilise une triple liaison 📋. Ces distinctions mettent en lumière la force et la stabilité relatives de chaque liaison.
Les paires d’électrons : liantes et non-liantes
Dans une structure de Lewis, les électrons sont divisés en paires d’électrons liantes et non-liantes. Les premières sont partagées entre les atomes pour constituer des liaisons, alors que les secondes restent sur un seul atome, influençant la forme et la polarité des molécules.
Pour la molécule d’eau, par exemple, les deux paires d’électrons non-liantes présentes sur l’oxygène affectent la géométrie en formant un angle de 104,5 degrés entre les liaisons OH, plutôt qu’une ligne droite.
Sur le meme sujet
La Puissance des Techniques Respiratoires pour Apaiser le Système Nerveux La respiration joue un rôle crucial pour maintenir notre système…
Pourquoi la méthode de Lewis est-elle si utile ?
La méthode de Lewis est non seulement une technique d’apprentissage, mais elle est également cruciale pour prévoir les interactions chimiques et les propriétés physiques des molécules. En visualisant comment les électrons de valence sont distribués, elle permet de comprendre pourquoi certaines molécules réagissent comme elles le font.
Elle offre également aux élèves une solide base pour aborder des concepts plus avancés comme la théorie des orbitales moléculaires ou les interactions VSEPR, qui étendent et approfondissent la compréhension de la chimie moléculaire.
Approfondir les connaissances avec des exemples concrets
Rien de tel que d’aborder ce concept avec des exercices pratiques 🎓. Prenons des composés simples tels que CH₄, NH₃ et SO₄²⁻, qui illustrent diverses configurations d’électrons et de liaisons pour donner aux étudiants la confiance nécessaire en ce domaine.
| Molécule | Liaisons | Paires non-liantes | Forme géométrique |
|---|---|---|---|
| Méthane (CH₄) 🍃 | 4 simples | 0 | Tétraédrique |
| Ammoniac (NH₃) 🧊 | 3 simples | 1 | Pyramide trigonal |
| Dioxyde de soufre (SO₂) 🌿 | 1 simple, 1 double | 1 | Angulaire |
Erreurs fréquentes et comment les éviter
Dans la représentation des structures de Lewis, plusieurs erreurs courantes peuvent survenir, surtout pour ceux qui découvrent pour la première fois cette méthode. Parmi celles-ci, on trouve l’oubli de la règle de l’octet ou l’ajout incorrect de liaisons ou d’électrons non-liants.
Un exercice utile est de vérifier si chaque atome satisfait son besoin d’atteindre la stabilité électronique appropriée, en particulier pour les molécules complexes ou avec des exceptions à cette règle ⭐.
Astuces pour réussir
Pour affiner votre compréhension, il est essentiel de pratiquer régulièrement. Utilisez des modèles moléculaires ou logiciels de chimie pour manipuler et visualiser les structures en trois dimensions, renforçant ainsi la compréhension des configurations d’électrons et des formes moléculaires.
Qu’est-ce que la règle de l’octet et pourquoi est-elle importante ?
Elle stipule qu’un atome est le plus stable entouré de huit électrons de valence, guidant ainsi la formation des liaisons chimiques.
Les structures de Lewis peuvent-elles représenter toutes les molécules ?
Elles sont idéales pour de nombreuses molécules mais ont des limitations pour des composés plus complexes ou excédentaires en électrons.
Comment différencier paires liantes et non-liantes ?
Les paires liantes participent aux liaisons entre atomes, tandis que les non-liantes influencent la polarité et la forme de la molécule.
Claire Dubreuil, fondatrice de Sciences Box, enseigne la physique-chimie au collège depuis plus de 15 ans. Spécialisée dans la pédagogie active, elle crée des contenus clairs et motivants pour aider ses élèves à progresser. Elle est la voix éditoriale principale du site, qu’elle a conçu pour prolonger la salle de classe en ligne.