I/- Quelle est la composition de l'air ?
Activité : la composition de l'air
Bilan :
L'air, comme toute la matière, est composé d'atomes et de molécules.
Une molécule est un assemblage d'atomes liés entre eux.
La formule chimique d'une molécule permet de donner sa composition atomique, c'est-à-dire le nombre de chaque type d'atome qui la compose.
Propriétés :
- Les formules des molécules utilisent les symboles des atomes.
- Si la molécule est composée du même atome plusieurs fois, alors ce nombre est indiqué en bas à droite du symbole de l'atome.
Bilan :
L'air est composé d'environ 20% de dioxygène et de 80% de diazote. On trouve également d'autres gaz, présents en plus petite quantité : dioxyde de carbone, argon, ...
II/- Comment modéliser la matière à l'échelle microscopique ?
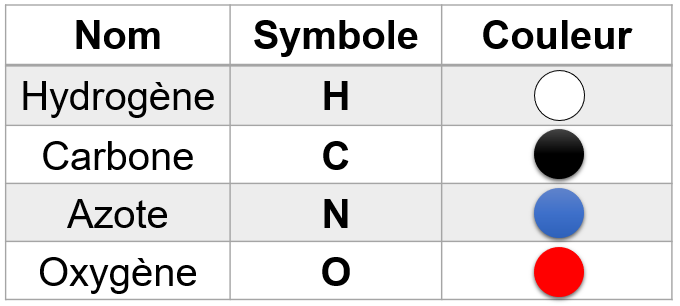
On représente les atomes par des sphères colorées (mais les atomes ne sont pas colorés en réalité, c'est un modèle).
Exemple :
L'eau est une molécule composée de deux atomes d'hydrogène et d’un atome d'oxygène.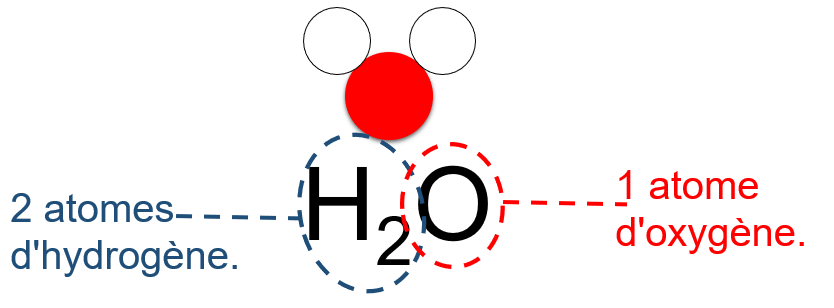
Bilan :
Pour modéliser l'air, on doit dessiner 4 fois plus de molécules de diazote que de molécules de dioxygène. Ces molécules sont très agitées (état gazeux) et mélangées (mélange homogène).
III/- L'air possède-t-il une masse ?
Activité p42
Bilan :
L’air possède une masse, comme toute la matière, quel que soit son état. Dans des conditions normales, 1L d’air possède une masse d’environ 1,3 g.
La fumée n’est pas un gaz, ni un liquide (contrairement aux nuages). La fumée est constituée de particules solides en suspension.
Application utilisée en activité expérimentale : Application à télécharger et marqueurs à imprimer
| App Store | Google Play | Les marqueurs à imprimer |
 |
 |
 |
| Programme de l'évaluation |
 |

