Les fondamentaux des états physiques de la matière
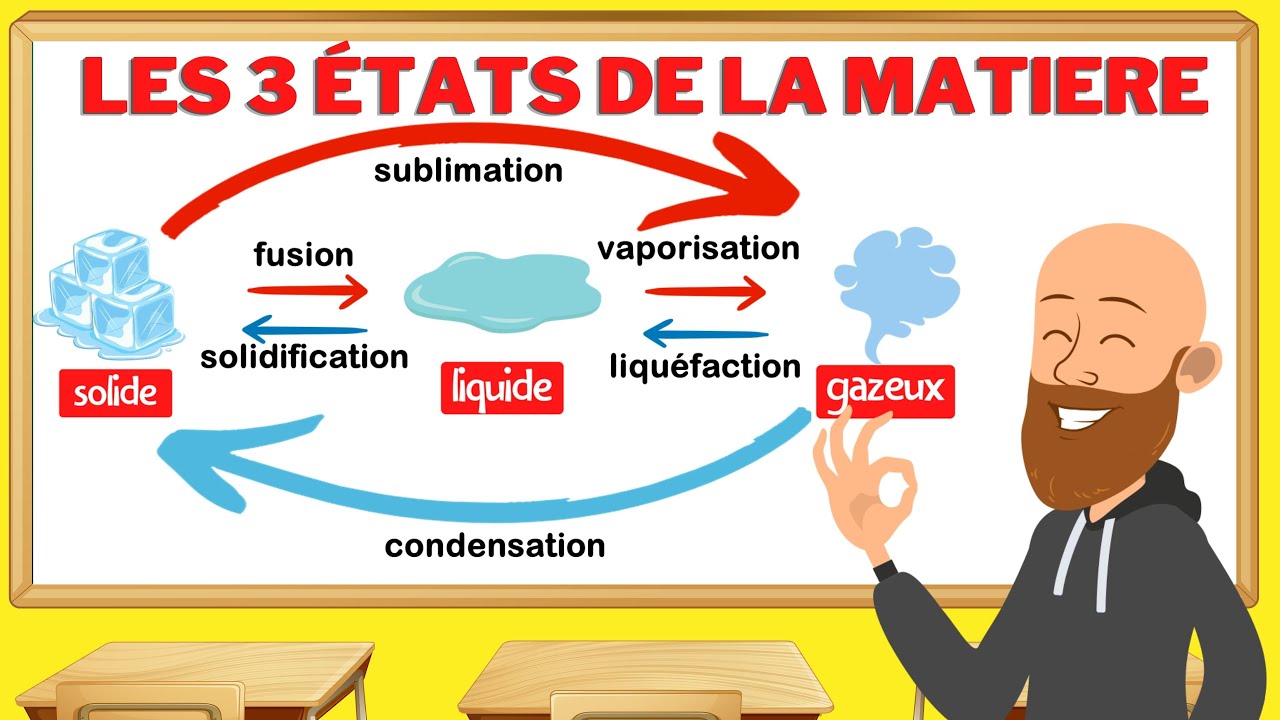
La matière qui nous entoure existe sous trois états physiques distincts : solide, liquide et gazeux. Prenons l’eau par exemple, elle se manifeste sous la forme de glace, d’eau liquide et de vapeur d’eau. Dans l’état solide, les molécules sont fortement liées, formant une structure rigide et ordonnée. En revanche, dans l’état liquide, ces mêmes molécules sont moins étroitement associées, leur permettant de se déplacer tout en restant relativement proches les unes des autres. Enfin, à l’état gazeux, les molécules se répartissent librement dans l’espace disponible, créant un milieu totalement désordonné.
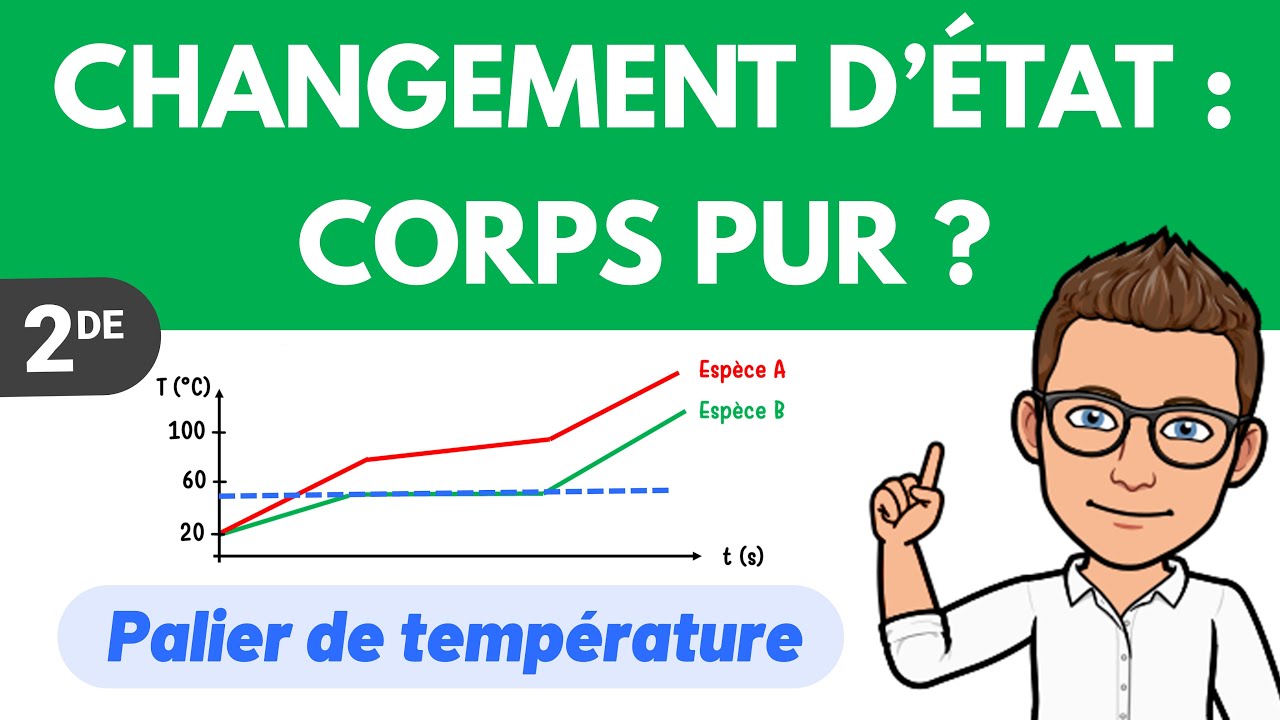
Pour bien comprendre ces états, il est crucial de se référer à des notions telles que la chaleur et la température, ces dernières jouant un rôle central dans la transformation d’un état à un autre. Par exemple, lorsque de la glace est chauffée et atteint zéro degré Celsius, elle se transforme en eau liquide dans un processus appelé fusion. Cela illustre l’importance de la température, qui détermine non seulement l’état physique d’un corps mais aussi ses changements potentiels.
Sur le meme sujet
Clermont-Ferrand : Un mariage entre art et science Dans le cadre enchanteur de Clermont-Ferrand, la fusion entre art et science…
Processus de fusion et de solidification
La transition de l’état solide à l’état liquide est connue sous le nom de fusion. Ce phénomène est tangible lorsqu’une substance solide, comme un glaçon, est exposée à une source de chaleur. La température à laquelle cette transition se produit est appelée température de fusion. À l’inverse, lorsque l’eau gèle, passant de l’état liquide à l’état solide, le processus est nommé solidification. Ce phénomène se produit généralement à des températures sous le point de congélation, soit zéro degré Celsius pour l’eau.
Un aspect fascinant de ces transformations est la conservation de la masse. Même si l’état et le volume changent, la masse totale de l’eau reste constante. Si l’on place une bouteille d’eau dans le congélateur, le volume occupé par l’eau sous forme de glace augmente, mais sa masse demeure inchangée. Ce phénomène est un exemple éclairant de la non-conservation du volume lors des changements de phase.
Pour aborder ces concepts de manière engagante et pédagogique, des ressources telles que ce site offrent des perspectives particulièrement riches pour explorer ces notions.
Sur le meme sujet
films de science-fiction incontournables pour les enfants dès 8 ans
Le voyage captivant dans l’univers de la science-fiction pour les jeunes Plonger les enfants dans l’univers des films de science-fiction…
Vaporisation et condensation : des processus énergétiques
Les phénomènes de vaporisation et de condensation sont essentiels à comprendre pour saisir le passage de l’état liquide à l’état gazeux et vice-versa. La vaporisation, qui inclut l’ébullition et l’évaporation, se produit quand une substance liquide absorbe suffisamment de chaleur pour s’évaporer entièrement. Cette transformation est observée lorsque l’eau atteint sa température d’ébullition à 100°C.
La condensation, à l’inverse, survient lorsque la vapeur se refroidit et retourne à l’état liquide. Ce processus est crucial dans de nombreux systèmes naturels et industriels, notamment dans le cycle de l’eau atmosphérique. La condensation est également visible sur les surfaces froides lorsqu’elles rencontrent de la vapeur d’eau, formant des gouttelettes.
Ces changements d’état illustrent l’importance de l’énergie thermique dans les transformations matérielles, et soulignent comment la température et la chaleur influencent la matière de manière significative.
Sur le meme sujet
Pourquoi les objets tombent-ils toujours vers le sol : comprendre la gravité
Les principes de la gravité : une force incontournable L’une des questions les plus fondamentales de la physique est celle…
Sublimation : un passage direct et remarquable
Le processus de sublimation est une transition directe de l’état solide à l’état gazeux, sans passer par l’état liquide. Un exemple typique est la glace sèche (CO₂ solide) qui se sublime à des températures ambiantes normales. Ce phénomène montre l’interaction complexe entre la température et la pression sur les substances solides susceptibles de se sublimer.
L’inverse de la sublimation est la déposition, où une substance passe directement de l’état gazeux à l’état solide. Ces transformations sont souvent utilisées dans des applications industrielles de haute technologie et nécessitent une compréhension approfondie des conditions thermodynamiques.
Les divers exemples de la vie quotidienne et les mises en situation pratiques aident à mieux appréhender ces phénomènes, nous rappelant comment la science est indissociable de notre environnement quotidien.
Facteurs influençant les changements d’état physique
La température et la pression sont les principaux facteurs influençant un changement d’état. À pression constante, chaque substance pure possède une température de changement spécifique pour chaque transition de phase. Cependant, en variant la pression, les températures des transitions peuvent également changer, démontrant la relation entre ces variables physiques.
Un motif clé ici est l’impact de la pression sur la température de fusion et d’ébullition. Par exemple, l’eau bouillira à une température inférieure à 100°C si l’on réduit la pression ambiante, un phénomène exploité dans des appareils tels que les autocuiseurs.
Cet équilibre thermodynamique souligne l’importance des conditions ambiantes dans les transformations physiques, rendant ces phénomènes plus compréhensibles et applicables à la vie quotidienne ainsi qu’à de nombreuses technologies.
L’importance de la conservation de l’énergie lors des changements d’état
Lors des transformations physiques, l’énergie est un élément clé. Lors d’une fusion ou d’une vaporisation, une quantité significative d’énergie est absorbée, tandis que lors d’une solidification ou d’une condensation, l’énergie est libérée. Ce transfert énergétique est une manifestation du premier principe de la thermodynamique, concernant la conservation de l’énergie.
Les implications de ces échanges énergétiques sont vastes, affectant des domaines aussi divers que la météorologie, la cuisine ou même la conception de systèmes de refroidissement. La compréhension de ces principes peut ainsi améliorer notre façon de gérer et exploiter la chaleur dans de nombreux contextes pratiques.
- 🌡️ Température critique pour les changements de phase
- 🎯 Utilisation pratique dans les technologies
- ⚙️ Applications industrielles et domestiques
Applications pratiques des changements d’état
Les changements d’état de la matière ne sont pas uniquement des concepts théoriques ; ils ont de nombreuses applications pratiques. Dans l’industrie alimentaire, le contrôle précis de la température et de la pression permet de stocker et transformer les produits de manière efficace. Les congélateurs domestiques fournissent une excellente illustration de la solidification contrôlée pour la conservation des aliments.
De même, les industries chimiques et pharmaceutiques exploitent ces principes pour développer des procédés de purification, de cristallisation et de synthèse. L’évaporation et la condensation sont au cœur des procédés distillatoires, utilisés pour séparer et purifier les liquides.
| 🔍 Processus | 📍 Applications | 🔬 Exemples |
|---|---|---|
| Fusion | Industrie alimentaire | Chocolat fondu |
| Vaporisation | Distillation | Production de pétrole |
| Condensation | Réfrigération | Climatisation |
Impact environnemental des changements d’état
Les transformations physiques de la matière ont également un impact environnemental considérable. Les processus industriels impliquant des changements d’état, comme la production de vapeur et la réfrigération, peuvent avoir des conséquences environnementales en termes d’énergie et d’émission de gaz à effet de serre.
Un exemple en est l’utilisation des réfrigérants dans les systèmes de climatisation, qui, s’ils ne sont pas correctement gérés, peuvent contribuer au réchauffement climatique. De plus, dans la nature, le cycle de l’eau est un système dynamique de changements d’état qui influence le climat mondial de manière profonde.
La prise de conscience de ces impacts incite à l’innovation pour développer des technologies plus durables, en témoignant de l’importance de la physique dans la lutte contre les problématiques environnementales.
Qu’est-ce qu’un changement d’état ?
Un changement d’état est une transformation physique par laquelle une matière passe d’un état (solide, liquide, gazeux) à un autre sous l’effet de modifications de température ou de pression.
Comment la température affecte-t-elle un changement d’état ?
La température est cruciale car elle détermine le moment où une substance changera d’état. Par exemple, l’eau gèle à 0°C et bout à 100°C à pression atmosphérique normale.
Quels sont les impacts des changements d’état sur l’environnement ?
Les processus industriels et naturels impliquant un changement d’état peuvent influencer l’environnement, notamment à travers l’émission de gaz à effet de serre et la consommation énergétique.
Claire Dubreuil, fondatrice de Sciences Box, enseigne la physique-chimie au collège depuis plus de 15 ans. Spécialisée dans la pédagogie active, elle crée des contenus clairs et motivants pour aider ses élèves à progresser. Elle est la voix éditoriale principale du site, qu’elle a conçu pour prolonger la salle de classe en ligne.